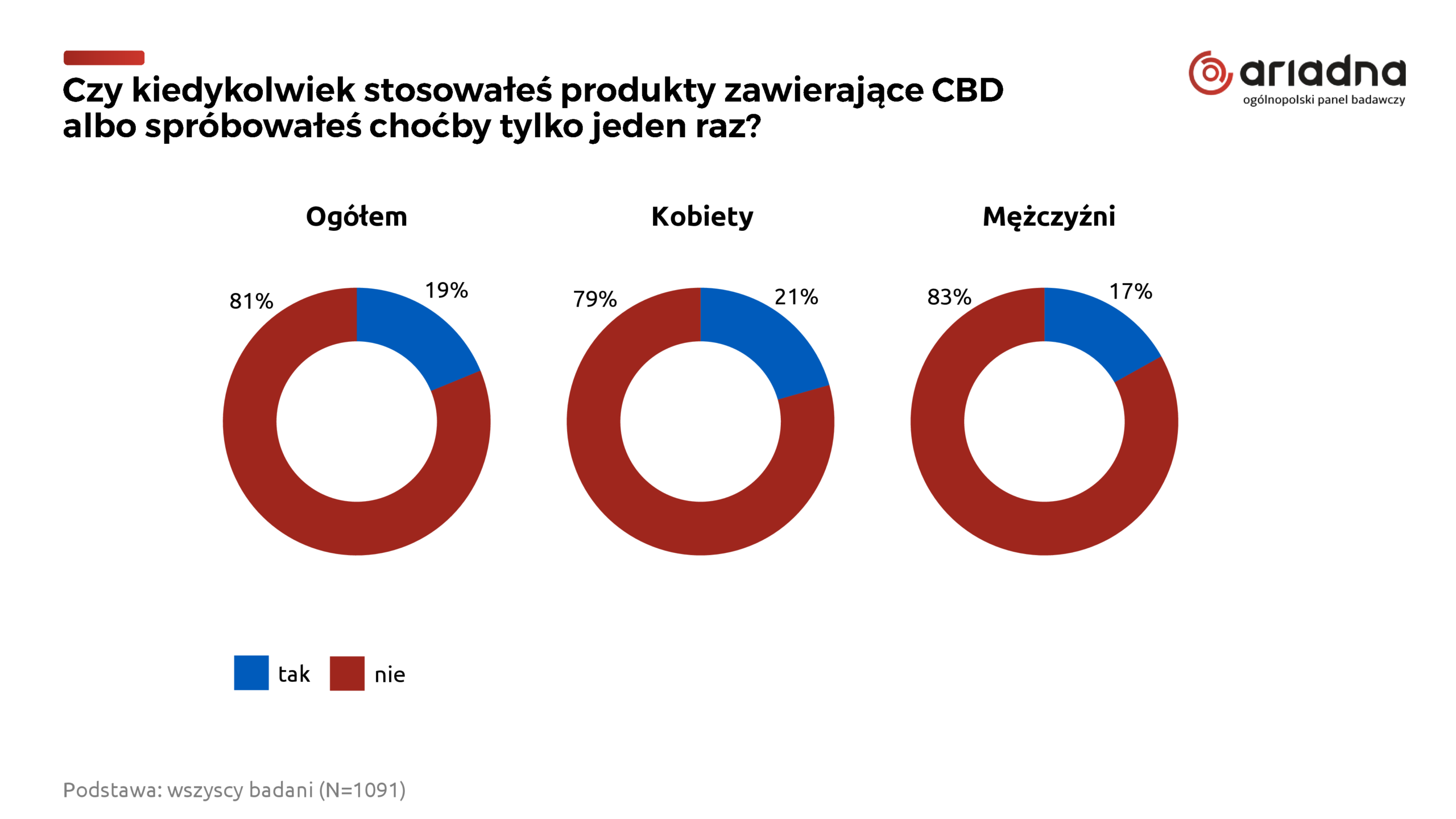
Główny Inspektorat Sanitarny i jego „eksperci” nie lubią konopi. Po wielu latach bezpodstawnych zarzutów, jakie stawiali przedsiębiorcom, w wytoczonej przez nas GIS-owi sprawie zapadł historyczny wyrok, który uciera im nosa i mówi wprost: konopie to nie „nowa żywność”.
Kiedy pierwszy raz wprowadzaliśmy do obrotu nasze „Zioła na Dobry Nastrój” , urzędnicy natychmiast przesłali do nas pismo, grożąc wyrokami i zabraniając nam sprzedaży tego produktu.
Co więcej, bez przeprowadzenia jakiegokolwiek postępowania zamieścili na swojej stronie internetowej adnotację, że produkt nie może znajdować się w obrocie. Nauczeni doświadczeniem złożyliśmy na nich skargę do sądu. Pierwsza rozprawa zakończyła się typowym niestety przyznaniem racji urzędnikom, w sposób do tego stopnia skandaliczny, że „uzasadnienie wyroku” zawierało nawet obszerne fragmenty przekopiowanych (razem z literówkami!) sformułowań GIS.
Nie poddając się, zaskarżyliśmy tę decyzję do Naczelnego Sądu Administracyjnego, który… przyznał nam rację, nakazując ponowne rozpatrzenie sprawy przez sąd niższej instancji.
Wyrok, który zapadł, jest bodaj pierwszym przypadkiem w Polsce (albo i w Europie!), w którym sąd nie ograniczył się do bezmyślnego przepisania stanowiska organu, a rzeczowo zapoznał się ze sprawą, po czym doszedł do jedynego wniosku, jaki można przyjąć, racjonalnie oceniając sprawę – że konopie nie są nową żywnością. Postanowienie to otwiera nam drogę do „kontrataku” – urzędnicy, który dopuścili się świadomych nadużyć, zatajeń i przeinaczeń zostaną teraz przez nas pociągnięci do osobistej odpowiedzialności.

Poniżej kilka „kwiatków” z uzasadnienia wyroku – a kto łasy większej ilości szczegółów, zachęcamy do zapoznania się z pełną treścią pisma umieszczoną niżej w tym artykule.
Organ administracji publicznej, ani sąd, orzekając ponownie w tej samej sprawie, nie mogą nie uwzględnić wykładni prawa dokonanej przez NSA
„roślina ta (…) ma historię stosowania i nie stanowi nowej żywności”
„Twierdzenie w tej sytuacji przez GIS, że (…) znana jest historia spożycia przed dniem 15 maja 1997 r. jako żywności tylko następujących produktów: nasion z konopi, oleju z nasion konopi, mąki z nasion konopi, odtłuszczonych nasion konopi, stanowiło nieuprawnioną nadinterpretację stanowiska Komisji Europejskiej”
„Dokonana przez GIS interpretacja zapisów Katalogu Nowej Żywności w kontekście „nowości” ziela Cannabis sativa L., jako żywności była wadliwa. Rację ma więc skarżąca, że stanowisko GIS jest błędne”
„Definitywne stwierdzenie „nowości” ziela Cannabis sativa L., jako żywności przez organ było niemożliwe także z tego powodu, że z przedłożonej przez skarżącą opinii Komisji Europejskiej z dnia 18 grudnia 1997 t., znanej także organowi z urzędu, wprost wynikało wyłączenie ziela Cannabis sativa L. spod obowiązywania rozporządzenia w sprawie nowej żywności. Wskazano w niej bowiem, że „zdecydowano, iż żywność zawierająca części ziela konopi siewnej nie podlega pod regulację (…) ws. Nowej żywności”
„(…) niewątpliwe dowody przedstawione przez stronę w ramach przedmiotowego postępowania wskazywały historię spożycia ziela konopi włóknistych zarówno jako żywności, jak i celem suplementacji normalnej diety”
„(…) organ najpierw wadliwie zinterpretował zapisy Katalogu Nowej Żywności (…) a następnie przeprowadził niepełne i ograniczone do minimum postępowanie dowodowe, pomijając przy tym dowody z dokumentów złożone przez skarżącą, a także dowody wytworzone przez sam organ i znane mu z urzędu”
Nie spodziewamy się oczywiście, że GIS pójdzie dzięki temu po rozum do głowy i pogodzi się z tym, że przez lata się mylił. Wierzymy jednak, że „prawda zwycięży”, więc robimy swoje dalej, a tymczasem cieszymy się i zachęcamy do dzielenia się tą dobrą nowiną z całą konopną bracią!
PS – nie byłoby tego wyroku, gdyby nie ogromny wkład pracy mojej małżonki, autorki merytorycznej części wszystkich naszych pism procesowych, dr inż. Beaty Plutowskiej, która od dobrych kilku lat gromadzi dowody nie tylko na „historię spożycia konopi”, ale także buduje pokaźną kartotekę nadużyć i karygodnych postępków urzędowych „ekspertów” – i nie zawaha się jej użyć!
Dziękuję Beatka, kocham Cię!
Autor: Maciej Kowalski
-
 Białko konopne BIO 200 g35.00 zł
Białko konopne BIO 200 g35.00 zł
Dla dociekliwych prezentujemy oryginalną treść wyroku:
Sygn. akt V SA/Wa 5258/21
WYROK W IMIENIU RZECZYPOSPOLITEJ POLSKIEJ
Dnia 17 lutego 2022 r.
Wojewódzki Sąd Administracyjny w Warszawie w składzie następującym:
Przewodniczący Sędzia WSA – Monika Kramek (spr.)
Sędzia WSA – Konrad Łukaszewicz
Sędzia WSA – Michał Sowiński
po rozpoznaniu na posiedzeniu niejawnym w dniu 17 lutego 2022 r. sprawy ze skargi Kombinatu Konopnego S.A. z siedzibą w Gronowie Górnym na akt Głównego Inspektora Sanitarnego z dnia 15 maja 2020 r. nr BŹ.SD.46.516.2020.WA. w przedmiocie zamiaru wprowadzenia środka spożywczego po raz pierwszy do obrotu
- uchyla zaskarżony akt;
- zasądza od Głównego inspektora Sanitarnego na rzecz Kombinatu Konopnego S.A. z siedzibą w Gronowie Górnym kwotę 697 zł (sześćset dziewięćdziesiąt siedem złotych) tytułem zwrotu kosztów postepowania sądowego.
Sygn. akt V SA/Wa 5258/21
UZASADNIENIE
Przedmiotem skargi Kombinat Konopny Spółka z o. o. w Gronowie Górnym (dalej: „Spółka”, „Strona” lub „Skarżąca”) jest akt Głównego Inspektora Sanitarnego (dalej: „GIS” lub „organ”) z 15 maja 2020 r. nr BŻ.SD.46.516.2020.WA.1 dotyczący uprawnień i obowiązków Strony wynikających z ustawy z dnia 25 sierpnia 2006 r. o bezpieczeństwie żywności i żywienia (Dz. U. z 2019 r. poz. 1252, ze zm. — dalej: „u.b.ż.ż.”).
Zaskarżony akt został wydany w następującym stanie faktycznym i prawnym.
GIS w piśmie z 15 maja 2020 r., skierowanym do Spółki w odpowiedzi na powiadomienie o zamiarze wprowadzenia po raz pierwszy do obrotu na terytorium Rzeczypospolitej Polskiej suplementu diety pn.: „Zioła Na Dobry Nastrój” wskazał, ke przedmiotem postępowania jest produkt, który w zalecanej dziennej porcji (tj. w 4 kapsułkach) zawiera: 1000 mg ziela konopi włóknistych (Cannabis sativa), 320 mg korzenia kozłka lekarskiego (Radix valerianae), 320 mg liścia melisy (Melissae folium), 360 mg oliwy z oliwek.
Organ przypomniał, że pismem z 28 stycznia 2020 r. zawiadomił o rozpoczęciu postępowania wyjaśniającego, o którym mowa w art. 30 ust. 1 u.b.ż.ż.
Wobec wątpliwości, czy produkt jest środkiem spożywczym oraz czy spełnia wymagania dla środka spożywczego, Skarżąca została wezwana do przedstawienia dokumentacji potwierdzającej, że ziele konopi było stosowane do celów żywienia człowieka w państwach członkowskich Unii Europejskiej przed dniem 15 maja 1997 r.
W piśmie z 26 lutego 2020 r. Spółka przedstawiła stanowisko w sprawie. Ponadto, mając na uwadze określony w wezwaniu przedmiot sprawy, tj. wątpliwości GIS co do stosowania ziela Cannabis sativa L. w żywności, w tym w suplementach diety, przed dniem 15 maja 1997 r. wniosła o przeprowadzenie dowodu z przesłuchania wskazanych świadków na okoliczność historii spożycia ziela Cannabis sativa L. w tym wprowadzania do obrotu ziela Cannabis sativa L. w znacznych ilościach przed 15 maja 1997 r. oraz przeprowadzenia dowodu z dokumentów załączonych do pisma tj. skanów ze strony internetowej Katalogu Nowej żywności dotyczących rośliny Cannabis sativa L. aktualnych na dzień 18 lutego 2020 r., 11 lutego 2018 r., 30 marca 2017 r. oraz dokumentów w których Komisja Europejska powołuje się opinię z 18 grudnia 1997 r. dotycząca tej rośliny.
W ocenie Strony w niniejszej sprawie nie doszło do spełnienia przesłanki uzasadniającej wszczęcie postępowania wyjaśniającego, o którym mowa w art. 30 ust. 1 u.b.ż.ż. Jest bowiem oczywiste, że ziele Cannabis sativa L. było stosowane w żywieniu przed 15 maja 1997 r., co potwierdzają liczne źródła wskazane w piśmie. Potwierdza to również Komisja Europejska bowiem w publikowanym przez nią Katalogu Nowej Żywności nie wskazano, aby ziele konopi włóknistych było nową żywnością. Brak jest również podstaw do żądania od Strony przedstawienia dokumentacji potwierdzającej historię stosowania ziela Cannabis sativa L. Przepis, na który powołał się GIS, tj. art. 121 ust. 1 u.b.ż.ż. stanowi bowiem, że podmiot działający na rynku spożywczym jest zobowiązany do przedstawienia dokumentacji potwierdzającej historię stosowania żywności jedynie w przypadku wątpliwości, czy żywność wprowadzana do obrotu była dotychczas stosowana w żywieniu ludzi. Spółka przedstawiła argumenty na okoliczność, że w Katalogu Nowej Żywności nie istnieją żadne przesłanki uprawniające do stwierdzenia, że ziele Cannabis sativa L. wykorzystywane w produkcie jest nową żywnością, a w związku z powyższym produkty spożywcze zawierające lub składające się z ziela Cannabis sativa L. nie są objęte zakresem rozporządzenia Parlamentu Europejskiego i Rady (UE) nr 2015/2283 z dnia 25 listopada 2015 r. w sprawie nowej żywności i nie jest konieczne przeprowadzenie postępowania w sprawie wydania zezwolenia na wprowadzenie nowej żywności na rynek w Unii Europejskiej.
Spółka wskazała na dowody na wykorzystanie ziela konopi Cannabis sativa L. jako surowca zielarskiego w żywności, dowody na wykorzystanie ziela konopi Cannabis sativa L. w żywności oraz opisała dokumenty świadczące o tym, że ziele Cannabis sativa L nie stanowi nowej żywności w rozumieniu rozporządzenia nr 2015/2283. Podniosła również zarzut braku działań wobec innych przedsiębiorców wprowadzających do obrotu podobne produkty.
Po przeanalizowaniu dowodów i argumentów przedstawionych przez Stronę, organ stwierdził, że nie są one wystarczające, aby potwierdzić historię znaczącego spożycia ziela konopi włóknistych w żywności w celu żywienia ludzi w państwach członkowskich UE. Zdaniem organu przedstawione dowody w większości przypadków wskazują bowiem, że ziele konopi było stosowane w celach leczniczych, a nie jako żywność. Zgodnie z regulacjami prawa żywnościowego, środki spożywcze, w tym suplementy diety nie mogą posiadać właściwości charakterystycznych dla produktów leczniczych w rozumieniu przepisów prawa farmaceutycznego.
Definicja żywności określona została w art. 2 rozporządzenia (WE) Nr 178/2002 Parlamentu Europejskiego i Rady z dnia 28 stycznia 2002 r. ustanawiającego ogólne zasady i wymagania prawa żywnościowego (…) (Dz. Urz. WE L 31 z 1.2.2002 r., s. 1, ze zm.). W przepisie tym wskazano, że środek spożywczy nie obejmuje m.in. produktów leczniczych w rozumieniu dyrektyw Rady 65/65/EWG (1) i 92/73/EWG; narkotyków lub substancji psychotropowych w rozumieniu konwencji o środkach odurzających z 1961 r. Oraz Konwencji o substancjach psychotropowych z 1971 r.
Odnosząc się do powoływanego przez Stronę dekretu Ministerstwa Rolnictwa i Rozwoju Wsi Republiki Słowackiej nr 309/2015, gdzie wśród szeregu surowców roślinnych, które mogą być stosowane w produkcji herbaty wymieniono liście i nasiona rośliny Cannabis sativa L. – organ wskazał, że może to ewentualnie dowodzić zastosowania liści i nasion w produkcji herbat (a nie całego ziela – kwiatów, liści, łodyg). Natomiast spożycie liści konopi w herbatach nie stanowi o „znaczącym spożyciu” ziela konopi w żywności, w tym w suplementach diety przed dniem 15 maja 1997 r.
W ocenie organu Strona dokonała błędnej interpretacji zapisów Katalogu Nowej Żywności prowadzonego przez Komisję Europejską, dotyczących konopi siewnych (Cannabis sativa L.). W Katalogu wskazano bowiem, że w przypadku rośliny Cannabis sativa L. znana jest historia spożycia przed dniem 15 maja 1997 r. jako żywności, tylko określonych produktów pochodzących z konopi: nasion, oleju z nasion konopi, mąki z nasion konopi, odtłuszczonych nasion konopi. Powyższe zapisy Katalogu znalazły odzwierciedlenie w opinii Komisji ds. Bezpieczeństwa Żywności i Żywienia Rady Sanitarno-Epidemiologicznej przy GIS z dnia 27 maja 2019 r., w sprawie bezpieczeństwa stosowania konopi siewnych w żywności ze względu na obecność THC i CBD. Brak jest danych na temat bezpieczeństwa pozostałych (oprócz nasion) części roślinnych pochodzących z konopi siewnych. W związku z tym składniki te są nową żywnością. Produkty pochodzące z innych części rośliny konopie siewne, uważane są za nową żywność.
Dalej organ wskazał, że na przestrzeni ostatnich lat status prawny Cannabis sativa L. oraz kannabinoidów był wielokrotnie weryfikowany oraz dyskutowany na posiedzeniach Komisji Europejskiej w ramach grupy roboczej ds. nowej żywności, a także grupy roboczej ds. aromatów. Obecne zapisy w Katalogu Nowej Żywności dotyczące statusu Cannabis sativa L. wypracowane zostały przez przedstawicieli poszczególnych państw członkowskich.
W posiedzeniach grupy roboczej ds. nowej żywności na poziomie Komisji Europejskiej brali również udział przedstawiciele European Industrial Hemp Association (EIHA), wraz ze swoimi współpracownikami, a także przedstawiciele brytyjskiego stowarzyszenia – Cannabis Trades Association UK. W związku z tym argumenty przedstawiane przez Stronę są znane.
Przed wprowadzeniem do obrotu na terytorium Unii Europejskiej (w tym Polski) jako żywności produktów zawierających w swoim składzie ziele konopi, konieczne jest przeprowadzenie postępowania w sprawie wydania zezwolenia na wprowadzenie nowej żywności na rynek Unii Europejskiej, określonego przepisami rozporządzenia nr 2015/2283 z dnia 25 listopada 2015 r. w sprawie nowej żywności, zmieniającego rozporządzenie Parlamentu Europejskiego i Rady (UE) Nr 1169/2011 oraz uchylającego rozporządzenie (WE) Nr 258/97 Parlamentu Europejskiego i Rady oraz rozporządzenie Komisji (WE) Nr 1852/2001 (Dz. Urz. UE L 327 z 11.122015 r, s. 1).
Zdaniem organu sugestie Strony, że Komisja ds. Bezpieczeństwa Żywności i Żywienia Rady Sanitarno – Epidemiologicznej przy Głównym Inspektorze Sanitarnym nadinterpretuje zapisy Katalogu Nowej Żywności, czy też nie ma wiedzy, co do składnika roślinnego – Cannabis sativa są bezpodstawne.
Stosownie do ustawy o Państwowej Inspekcji Sanitarnej z dnia 14 marca 1985 r. (Dz.U. z 2019 r., poz. 59, ze zm.) organem doradczym i opiniodawczym Głównego Inspektora Sanitarnego w sprawach objętych zakresem działania Państwowej Inspekcji Sanitarnej jest Rada Sanitarno-Epidemiologiczna. W ramach Rady działa m.in. Komisja ds. Bezpieczeństwa Żywności i Żywienia – jako organ opiniodawczo-doradczy Głównego Inspektora Sanitarnego. Osoby wchodzące w skład Rady są pracownikami nauki posiadającymi wybitne przygotowanie praktyczne z dziedziny sanitarno-epidemiologicznej. Wśród nich znajdują się krajowi eksperci biorący udział w grupach roboczych Komisji Europejskiej z zakresu prawa żywnościowego oraz w pracach Europejskiego Urzędu ds. Bezpieczeństwa Żywności (EFSA).
Poza wskazanym statusem prawnym wprowadzanego na rynek produktu „Zioła Na Dobry Nastrój”, zawierającego ziele rośliny Cannabis sativa L., istotna była zdaniem organu kwestia bezpieczeństwa stosowania konopi siewnych i produktów z nich otrzymywanych jako żywności. Organ stwierdził, że wprowadzanie do obrotu jako żywność, suszu z konopi siewnych może stanowić potencjalne zagrożenie dla konsumenta ze względu na zawartość THC, ponieważ wszystkie części rośliny konopi siewnych mogą zawierać fitokannabinoidy. Najwyższe stężenie fitokannabinoidów występuje w kwiatostanach i liściach („Cannabis sativa: the plant ofthe thousand and one molecules”. Andre C.M. et al. Front Plant Sci. 2016; 7:19). Jednym z fitokannabinoidów jest A9-THC, który wykazuje silne działanie psychoaktywne na organizm człowieka.
Substancja oddziałuje na centralny układ nerwowy powodując m.in. zwiększenie czynności serca (tachykardię), zmiany nastroju. Chroniczne narażenie na THC wpływa na centralny układ nerwowy powodując upośledzenie motoryki, ograniczenie zachowań społecznych, upośledzenie procesów uczenia się, spadek masy ciała, upośledzenie spermatogenezy, zmiany histopatologiczne oraz szkodliwe działanie na układ odpornościowy.
Organ podniósł, że Europejski Urząd ds. Bezpieczeństwa Żywności (EFSA) w raporcie z dnia 7 stycznia 2020 r. Acute human exposure assessment to tetrahydrocannabinol (EFSA Journal 2020; 18(1):5953) ocenił m.in., że spożycie herbatki z konopi siewnych na poziomie wysokiego spożycia, wiąże się z ekspozycją na 2080% ustalonej dawki referencyjnej. EFSA w 2015 r. dokonał oceny ryzyka dla zdrowia człowieka związanego z obecnością tetrahydrokannabinoli (THC) w mleku i innych produktach pochodzenia zwierzęcego. Określono ostrą dawkę referencyjną dla ludzi wynoszącą 1 pg A9-THC/kg m,c. Biorąc pod uwagę ten parametr toksykometryczny, w przypadku konsumentów dorosłych, dzienne pobranie A9-THC nie przekraczające 70 pg nie stwarza istotnego ryzyka dla zdrowia.
Dalej organ wskazał, że Komisja ds. Bezpieczeństwa Żywności w opinii z 27 maja 2019 r. zwróciła uwagę m.in., że w przypadku stwierdzenia w produktach z konopi siewnych THC, konieczne jest każdorazowe dokonanie oceny ryzyka, na podstawie przyjętej przez EFSA ostrej dawki referencyjnej (ARfD), 1 pg A9- THC/kg m.c. (pkt 3 opinii). Komisja zaleciła, aby zawartość THC w produktach otrzymanych z konopi siewnych była badana przez przedsiębiorcę w ramach procedur wewnętrznych tak, aby dokonać oceny narażenia konsumentów.
W rozpoznawanej sprawie brak jest wyników analizy przedmiotowego produktu na obecność i zawartość A9-THC.
Zastrzeżenie organu wzbudziła także zawartość w składzie produktu „Zioła Na Dobry Nastrój”, korzenia kozłka lekarskiego oraz liścia melisy w dawce terapeutycznej. Zgodnie z monografią EMA z dnia 14 maja 2013 r. dotyczącą Melissa officinalis, folium dawkę terapeutyczną stanowi 0,19 – 0,55 g sproszkowanej substancji roślinnej stosowanej 2-3 razy dziennie. Natomiast według monografii EMA, z dnia 2 lutego 2016 r. dotyczącej Valeriana officinalis, radix dawkę terapeutyczną stanowi 0,3 – 3 g rozdrobnionej substancji roślinnej stosowanej do 3 razy dziennie. Organ wskazał też na możliwość wystąpienia działania synergistycznego ziela konopi włóknistej, kozłka lekarskiego oraz melisy lekarskiej, co może prowadzić do spotęgowania właściwości produktu.
W skardze na akt GIS z 15 maja 2020 r. Skarżąca domagając się uchylenia zaskarżonego aktu oraz umorzenia postępowania wyjaśniającego zarzuciła:
1. naruszenie przepisów postępowania:
- art. 7, 77 i 80 k.p.a., poprzez przeprowadzenie niepełnego postępowania dowodowego oraz dowolną ocenę zgromadzonego materiału dowodowego, powołanie nieadekwatnej opinii organu doradczego – skutkującej ustaleniem, że sproszkowane ziele Cannabis sativa L. stanowi nową żywność i konieczne jest przeprowadzenie europejskich procedur rejestracyjnych;
- art. 7a k.p.a., poprzez rozstrzygnięcie ewentualnych wątpliwości na niekorzyść strony, pomimo stanowiska Komisji Europejskiej z dnia 18 grudnia 1997 r. oraz danych wynikających z internetowego Katalogu Nowej żywności UE – niewłaściwe uznanie, że Cannabis sativa L. stanowi nową żywność;
- art. 8 k.p.a., poprzez przeprowadzenie postępowania w sposób niebudzący zaufania do władzy publicznej oraz godzący w zasadę równego traktowania, czego przejawem jest wszczęcie postępowania wyjaśniającego, co do statusu Cannabis sativa L. jako nowej żywności bez przeanalizowania argumentów strony, wobec ponad stu produktów oferowanych aktualnie na rynku, zawierających w składzie ziele Cannabis sativa L.;
2. naruszenie prawa materialnego, tj. art. 6 ust. 2 rozporządzenia UE ws. nowej żywności, poprzez jego niewłaściwe zastosowanie do wadliwie ustalonego stanu faktycznego i w konsekwencji błędne uznanie, że składnik produktu Cannabis sativa L. wymaga zezwolenia na wprowadzenie na rynek Unii i stanowi nową żywność, wymagającą przeprowadzenia procedury rejestracyjnej.
W uzasadnieniu skargi wskazano, że GIS wszczął postępowanie na podstawie art. 30 ust. 1 u.b.ż.ż., po dokonaniu przez Stronę zawiadomienia, o którym mowa w art. 29 ust. 1 ustawy. Pierwsze pismo GIS wystosował w dniu 30 grudnia 2019 r., pomimo że formalnie nie wszczął wówczas postępowania. Organ wyraził stanowisko, że produkt pn. „Zioła na dobry nastrój”, z uwagi na zawartość sproszkowanego ziela konopi włóknistych Cannabis sativa L. stanowi nową żywność, wymagającą przeprowadzenia postępowania ws. zezwolenia na wprowadzenie nowej żywności na rynek.
W rejestrze produktów objętych powiadomieniem o pierwszym wprowadzeniu do obrotu, publikowanym na stronie internetowej GIS – pojawiła się przy produkcie Strony adnotacja: produkt, nie może zostać wprowadzony do obrotu jako środek spożywczy.
Państwowy Powiatowy Inspektor Sanitarny w Elblągu przeprowadził w dniu 15 stycznia 2020 r. w zakładzie strony kontrolę sanitarną, po czym w dniu 27 stycznia 2020 r. wszczął postępowanie w przedmiocie „wycofania z obrotu handlowego produktu pn. Zioła na dobry nastrój “. GIS w dniu 5 lutego 2020 r. zmodyfikował w swoim Rejestrze, status produktu strony na zapis: „zawiera składnik niedozwolony”. Powyższe działania zostały podjęte bez formalnego wszczęcia postępowania wyjaśniającego.
Następnie GIS wszczął postępowanie wyjaśniające, wskazując na brak dowodów na historię spożycia ziela Cannabis sativa L. przed 15 maja 1997 r. Organ wezwał stronę do „przedstawienia dokumentacji potwierdzającej, że ziele konopi włóknistych było stosowane do celów żywienia człowieka w państwach członkowskich UE przed tym dniem.
Spółka złożyła obszerne wyjaśnienia i zaoferowała przesłuchanie siedmiu świadków – ekspertów na okoliczność, że ziele Cannabis sativa L. było w dużej mierze spożywane przed 15 maja 1997 r. Wniosku tego organ nie uwzględnił.
Zdaniem strony, organ wadliwie interpretuje treść internetowego Katalogu Nowej Żywności publikowanego przez Komisję Europejską. Uznał bowiem, że z opisu pod hasłem Cannabis sativa L. wynika, że jej części nadziemne, stanowią nową żywność.
Tymczasem roślina Cannahis sativa L. została oznaczona zieloną grafiką w kształcie litery „y”, co oznacza status żywności dopuszczonej do obrotu. Roślina konopie włókniste (Cannabis sativa L.) to – liście, łodyga, kwiaty i nasiona. Nie ma podstaw do rozróżniania dopuszczalności obrotu suszem liści, łodyg czy kwiatów, skoro cała roślina w Katalogu została oznaczona zieloną ikoną. Jest zatem dopuszczona do obrotu na rynku Unii, bez potrzeby przeprowadzania procedury autoryzacji. Czerwonym symbolem „X” Katalog Nowej żywności UE oznaczył jedynie:
– ekstrakty z rośliny Cannabis sativa L. zawierające kannabinoidy,
- produkty pochodzące z tych ekstraktów, a więc wszelkie produkty, do których te ekstrakty zostały dodane (takie jak np. olej z nasion),
– ekstrakty z innych roślin niż Cannabis sativa L. zawierające kannabinoidy,
- syntetycznie otrzymane kannabinoidy.
Na bezpieczeństwo żywienia z wykorzystaniem ziela konopi, wpływa zawartość substancji aktywnych biologicznie – kannabinoidów: THC i CBD, których stosowanie budzi kontrowersje. Jednak CBD zostało uznane przez WHO za całkowicie bezpieczne. Niektóre produkty z roślin uzyskane w ramach działań fizykochemicznych, mają zwiększone stężenia tych związków. Dlatego tylko one wymagają osobnych procedur rejestracyjnych, na co wskazuje opis w unijnym katalogu Novei Food, znajdujący się przy haśle „Cannabinnoids”. Tylko te produkty unijny katalog oznaczył jako „nową żywność” i brak jest podstaw, aby rozciągać to na produkty, których bazowym surowcem jest ziele konopi włóknistych. Aktualnie, jako nowa żywność, zostały wymienione grupy produktów, w których na skutek dalszego przetwarzania rośliny, stężenia kannabinoidów są celowo zwiększane.
Zdaniem Skarżącej organ dysponował przedłożoną opinią Komisji Europejskiej z 18 grudnia 1997 r., która wskazywała na wyłączenie ziela Cannabis sativa L. spod obowiązywania rozporządzenia UE wers. nowej żywności. Strona przedstawiła też spis publikacji, w których wskazuje się na spożycie ziela konopi włóknistych od setek, a nawet tysięcy lat oraz zaoferowała dowody ze świadków, którzy potwierdziliby ten stan.
Organ powołał się na rzekome „niebezpieczeństwo” produktu z uwagi na zawartość THC, a nawet kozłka lekarskiego i melisy. Produkt zawiera niewiefe THC i należałoby spożywać codziennie nawet kilkadziesiąt kilogramów, ażeby przekroczyć poziom wynikający z opinii EFSA.
W odpowiedzi na skargę Spółki GIS wniósł o jej oddalenie wskazując, że 18 listopada 2019 r. Strona złożyła w Elektronicznym Systemie Powiadamiania, na podstawie art. 29 ust. 1 u.b.2.2 powiadomienie o zamiarze wprowadzenia po raz pierwszy do obrotu na terytorium Rzeczypospolitej Polskiej produktu pn.: „Zioła na dobry nastrój””, który zakwalifikowała jako suplement diety.
W powiadomieniu, o którym mowa w art. 29 ust. 1 ustawy istnieje możliwość wybrania rodzaju powiadomienia: o wprowadzeniu środka spożywczego lub o zamiarze wprowadzenia środka spożywczego. Dwojakie rozwiązanie wynika z faktu, że nie każdy przedsiębiorca w momencie przesyłania powiadomienia, od razu wprowadza produkt do obrotu. Niektórzy przedsiębiorcy przed wprowadzeniem danego produktu na rynek, najpierw powiadamiają o zamiarze jego wprowadzenia na terytorium Rzeczypospolitej Polskiej. W tym przypadku strona zdecydowała się na powiadomienie o zamiarze wprowadzenia po raz pierwszy na terytorium RP produktu „Zioła na dobry nastrój”, co może wskazywać, że przedsiębiorca dopiero po uzyskaniu stanowiska GIS planował wprowadzenie go na rynek. Dalej wskazano, że od 17 lipca 2019 r. na stronie Głównego inspektoratu Sanitarnego zamieszczona jest opinia Komisji ds. Bezpieczeństwa Żywności i Żywienia Rady Sanitarno-Epidemiologicznej przy Głównym Inspektorze Sanitarnym w sprawie bezpieczeństwa stosowania konopi siewnych w żywności ze względu na obecność THC i CBD.
Pismem z 30 grudnia 2019 r. GIS poinformował Spółkę, że ze względu na obecność w produkcie ziela konopi (Cannabis sativa L), które zgodnie z informacją podaną w Katalogu Nowej Żywności, uznawane jest za nową żywność, produkt „Zioła na dobry nastrój” nie może być wprowadzony do obrotu na terytorium RP jako środek spożywczy. Przed wprowadzeniem produktu na rynek Unii Europejskiej jako żywności, niezbędne jest przeprowadzenie postępowania w sprawie wydania zezwolenia na wprowadzenie nowej żywności na rynek Unii Europejskiej, zgodnie z przepisami rozporządzenia UE Nr 2015/2283 ws. nowej żywności. Przywołany został art. 3 ust. 2 lit a (iv) rozporządzenia UE Nr 2015/2283 dotyczący nowej żywności, do której zaliczyć należy konopie siewne.
Strona zwróciła się do GIS, aby usunąć z rejestru produktów, w rubryce „wynik postępowania”, błędną informację „nie może zostać wprowadzony do obrotu jako środek spożywczy”, gdyż nie zostało przeprowadzone, ani wszczęte żadne postępowanie wyjaśniające.
W odpowiedzi GIS zawiadomił stronę o rozpoczęciu postępowania wyjaśniającego, na podstawie art. 30 ust. 1 ustawy o bezpieczeństwie żywności i żywienia. Zdaniem GIS brak jest danych potwierdzających stosowanie ziela konopi włóknistych w żywności, w tym w suplementach diety, w celu żywienia ludzi w państwach członkowskich Unii Europejskiej przed dniem 15 maja 1997 r.
W rejestrze GIS zamieszczono wpis „postępowanie w toku” – zgodnie z rozporządzeniem Ministra Zdrowia z dnia 21 grudnia 2019 r. zmieniającym rozporządzenie w sprawie wzoru formularza powiadomienia o produktach wprowadzanych po raz pierwszy do obrotu na terytorium Rzeczypospolitej Polskiej, rejestru produktów objętych powiadomieniem oraz wykazu krajowych jednostek naukowych właściwych do wydawania opinii (Dz.U. z 2019r., poz. 2499).
W ocenie GIS argumentacja strony nie była wystarczająca do potwierdzenia historii znaczącego spożycia ziela konopi siewnych w żywności w celu żywienia ludzi w państwach członkowskich UE przed dniem 15 maja 1997 r. Zdaniem organu, to strona błędnie interpretuje widniejące od stycznia 2019 r. zapisy w Katalogu Nowej Żywności, w odniesieniu do rośliny konopie siewne (Cannabis sativa L.). Obecne stanowisko Komisji Europejskiej zamieszczone w Katalogu Nowej żywności dotyczące rośliny Cannabis sativa L. pojawiło się na początku 2019 r., po przeprowadzeniu na przestrzeni kilku lat uzgodnień w ramach grupy roboczej KE ds, nowej żywności, a także grupy roboczej KE ds, aromatów. Z Katalogu Nowej żywności wynika, że w przypadku rośliny Cannabis sativa L. znana jest historia spożycia przed dniem 15 maja 1997 r. jako żywności określonych produktów z konopi, tj.: nasion z konopi, oleju z nasion konopi, mąki z nasion konopi, odtłuszczonych nasion konopi. Wśród podanych w Katalogu Nowej Żywności produktów nie występują pozostałe części rośliny Cannabis sativa L (w postaci ziela, czyli kwiatostanów, liści i łodyg). Składniki te uważane są za nową żywność, ze względu na brak danych na temat ich bezpiecznego stosowania w państwach członkowskich UE.
Organ wskazał, że w niektórych państwach członkowskich stosowanie konopi siewnych w żywności jest zabronione. W Belgii roślina Cannabis sativa L. została umieszczona na liście pod nr 1 „Niebezpieczne rośliny, które nie mogą być wykorzystane jako żywność lub składnik żywności”. We Francji roślina Cannabis sativa L nie została wymieniona wśród składników roślinnych dozwolonych do stosowania w grupie żywności. Zgodnie z przepisami prawa żywnościowego obowiązującymi we Włoszech, do suplementów diety wolno stosować jedynie nasiona oraz olej z nasion rośliny Cannabis sativa L. W Bułgarii w suplementach diety można stosować jedynie nasiona z Cannabis sativa L. W Niemczech jedynie nasiona wymienione są jako część rośliny Cannabis sativa L. którą można stosować do żywności (znana jest historia spożycia). Powoływany przez stronę dekret Ministerstwa Rolnictwa i Rozwoju Wsi Republiki Słowackiej nr 30912015, wskazuje na możliwość stosowania do produkcji herbaty liści i nasion pochodzących z rośliny Cannabis sativa L. Zastosowanie to może być dowodem na historię spożycia herbaty zawierającej liście Cannabis sativa L., a nie całego ziela (liści, łodyg i kwiatostanów). Różne podejście poszczególnych państw Unii Europejskiej wskazuje, że ziele konopi Cannabis sativa L. nie jest dozwolone do stosowania jako żywność w poszczególnych państwach członkowskich. Stanowisko Komisji Europejskiej zamieszczone w Katalogu Nowej żywności w odniesieniu do innych części konopi siewnych (Cannabis sativa L.) niż nasiona jest jednoznaczne. Przed wprowadzeniem do obrotu na terytorium Unii Europejskiej jako żywności ziela konopi siewnych niezbędne jest przeprowadzenie postępowania w sprawie wydania zezwolenia na wprowadzenie nowej żywności na rynek unijny na podstawie rozporządzenia UE Nr 2105/2283 ws. nowej żywności. Ocenę tę potwierdza szereg wniosków złożonych do Komisji Europejskiej dotyczących produktów z konopi Cannabis sativa L. jako nowej żywności, składanych przez wnioskodawców za pośrednictwem elektronicznego systemu składania wniosków, tzw. „e-submission system”. W chwili obecnej zostało złożonych przez różnych przedsiębiorców około 60 wniosków dotyczących produktów otrzymywanych z konopi Cannabis sativa L., w tym kannabidiolu (CBD). Stanowisko Komisji ds. Bezpieczeństwa Żywności i Żywienia Rady Sanitarno-Epidemiologicznej przy GIS z 27 maja 2019 r., w sprawie bezpieczeństwa stosowania konopi siewnych w żywności ze względu na obecność THC i CBD jest prawidłowe.
W odniesieniu do zarzutu „rzekomego niebezpieczeństwa produktu z uwagi na zawartość THC”, GIS podkreślił, że nie stwierdził, by produkt był niebezpieczny, ale zwrócił uwagę na fakt, że w złożonej przez stronę dokumentacji nie ma wyników badań produktu w kierunku zawartości A9-THC – substancji psychoaktywnej. Rolą GIS nie jest przeprowadzanie dowodów na bezpieczeństwo czy na niebezpieczeństwo środków spożywczych. Unijnym urzędem powołanym do oceny ryzyka w zakresie bezpieczeństwa żywności jest Europejski Urząd ds. Bezpieczeństwa Żywności (EFSA).
Organ podniósł, że z informacji widniejących na stronach internetowych skarżącego https://wp.kombinatkonopny.pliproduktiziolanadobrynastroj/ wynika, że w składzie produktu znajdują się konopie włókniste (Cannabis sativa) poddane specjalnej procedurze technologicznej – dekarboksylacji. Dekarboksylacja przekształca kannabinoidy w ich aktywne formy, dzięki czemu można korzystać z pełni ich potencjału. Na stronie https://wp.kombinatkonopny.pl/dekarboksylacja-konopi/ znajduje się opis dekarboksylacji suszu konopnego. Susz konopny po dekarboksylacji może zawierać 8,77 % THC.
GIS ponowił zastrzeżenia, co do zawartości w składzie produktu korzenia kozłka lekarskiego oraz liści melisy (odpowiednio po 320 mg w zalecanej dziennej porcji – tj. w 4 kapsułkach). Taka ilości składników w produkcie, może wskazywać na właściwości terapeutyczne. Tymczasem suplement diety nie może wykazywać właściwości produktu leczniczego, co wynika z definicji suplementu diety zawartej art. 3 ust. 3 pkt 39 u.b.ż.ż.
Zgodnie z art. 2 lit. d, g rozporządzenia (WE) Nr 178/2002 Parlamentu Europejskiego i Rady z dnia 28 stycznia 2002 r. ustanawiającego ogólne zasady i wymagania prawa żywnościowego, powołującego Europejski Urząd ds. Bezpieczeństwa Żywności oraz ustanawiającego procedury w zakresie bezpieczeństwa żywności (Dz. Urz. WE L 31 z dnia 1.02.2002 r., z późn. zm.) „środek spożywczy” nie obejmuje produktów leczniczych, narkotyków lub substancji psychotropowych w rozumieniu konwencji o środkach odurzających z 1961 r. oraz Konwencji o substancjach psychotropowych z 1971 r.
Odnosząc się do zarzutu braku równego traktowania wszystkich przedsiębiorców wprowadzających do obrotu produkty zawierające Cannabis sativa L., GIS wskazał, że ze względu na dużą liczbę powiadomień „o zamiarze wprowadzenia do obrotu” w pierwszej kolejności analizowane są produkty, które zostały już wprowadzone do obrotu lub zostały zidentyfikowane w obrocie w ramach urzędowej kontroli żywności.
W odniesieniu do zarzutów naruszenia art. 7, art. 7a, art. 8, art. 77 oraz art. 80 k.p.a., GIS wskazał, że ocenione i zweryfikowane zostały wszystkie informacje uzyskane od strony.
W odniesieniu do zarzutu naruszenia prawa materialnego – art. 6 ust. 2 rozporządzenia UE nr 2015/2283 dotyczącego nowej żywności, GIS wyjaśnił, że produkt „Zioła na dobry nastrój” wobec zawartości ziela Cannabis sativa L., stanowi nową żywność.
W piśmie z 15 września 2020 r. stanowiącym replikę na odpowiedź organu na skargę Spółka nie zgodziła się z oceną, co do pełnego i szczegółowego odniesienia się do twierdzeń i dowodów zaoferowanych w toku sprawy. Organ de facto nie ocenił, a w części w ogóle nie przeprowadził przedstawionych dowodów, lecz jedynie polemizował z twierdzeniami, broniąc swojej wąsko uargumentowanej, odmiennej koncepcji.
Spółka nie zgodziła się z poglądem GIS, że Katalog Nowej Żywności UE można jedynie interpretować dychotomicznie. W jej ocenie Katalog z założenia nie wymienia wszystkich produktów żywnościowych oraz ich składników, jakie mogą być wykorzystywane do produkcji żywności. Fakt, że dany produkt spożywczy lub składnik nie jest w nim wprost wymieniony, nie świadczy o tym, że automatycznie jest on nową żywnością. W Katalogu Nowej Żywności są wymienione wyłącznie te produkty i składniki, co do których KE dostała zapytanie o opinię, czy dany produkt lub składnik powinien przejść procedurę autoryzacji. Mówi o tym wprost legenda objaśniająca status poszczególnych składników.
Spółka kolejny raz podkreśliła, że w opinii Komisji Europejskiej wyłącznie produkty i składniki wymienione wprost w Katalogu oraz dodatkowo oznaczone symbolem X mogą wymagać autoryzacji przed wprowadzeniem do obrotu jako nowa żywność.
Według Strony GIS próbuje manipulować oceną Sądu argumentując wybiórczo i podając nieprawdziwe twierdzenia, jakoby w niektórych państwach członkowskich stosowanie konopi siewnych było zabronione. Dodała, że GIS początkowo twierdził jedynie, że ziele konopi jest nową żywnością, zaś kiedy Strona przedstawiła dowody na to, że tak nie jest – to dopiero wówczas zaczął także argumentować, jakoby istniały przepisy zabraniające wykorzystania ziela konopi włóknistych Cannabis sativa L. z powodu ich niebezpieczeństwa dla zdrowia. GIS podał przy tym kompletnie nieadekwatne do sytuacji dane na temat szkodliwości THC oraz zaprezentował nietrafione przykłady ze „starannie” dobranych dokumentów pochodzących z kilku państw członkowskich UE. Nie ulega jednak wątpliwości, że GIS nie przedstawił ani jednego przepisu powszechnie obowiązującego prawa, który zabraniałby wykorzystania ziela konopi włóknistych do produkcji żywności w Polsce.
W ocenie Spółki wszelkie próby GIS utrudnienia lub zatrzymania swobodnej sprzedaży i przepływu żywności, w tym suplementów diety w UE, są także sprzeczne z zasadą swobody przepływu towarów w UE oznaczoną traktatami, ale i doprecyzowaną dorobkiem orzeczniczym Trybunału Sprawiedliwości, który rozszerza owe swobody także o zasadę wzajemnego uznania standardów.
Organ w piśmie procesowym z 21 stycznia 2021 r. podtrzymał stanowisko zawarte w odpowiedzi na skargę stwierdzając, że w replice Strona w większości powtarza zarzuty podniesione już w skardze z 29 czerwca 2020 r. na akt z 15 maja 2020 r. W jego ocenie w zaskarżonym piśmie w sposób wyczerpujący i prawidłowy został wyjaśniony stan faktyczny. Strona została poinformowana o podjętych krokach. W trakcie postępowania prowadzonego przez GIS ocenione zostały wszystkie informacje w zakresie korespondencji wymienianej między Stroną, a GIS. Ponadto GIS wykazał, że nie doszło do błędu w stwierdzeniu, że produkt Strony „Zioła na dobry nastrój” w zakresie składnika w postaci ziela Cannabis sativa L. stanowi nową żywność i że naruszone zostało unijne prawo żywnościowe w ww. zakresie.
Wyrokiem z 29 stycznia 2021 r. sygn. akt. VII SA/Wa 1439/20 Wojewódzki Sąd Administracyjny w Warszawie oddalił skargę podzielając ocenę organu, że produkty pochodzące z innych niż nasiona części rośliny konopie siewne, uważane są za nową żywność. Sąd I instancji wskazał, ze zgodnie z art. 3 ust. 2 lit. a Parlamentu Europejskiego i Rady (UE) Nr 2015/2283 z dnia 25 listopada 2015 r. w sprawie nowej żywności, „nowa żywność” to żywność, której nie stosowano w znacznym stopniu w Unii do spożycia przez ludzi przed dniem 15 maja 1997 r., która zalicza się do co najmniej jednej ze wskazanych kategorii. Może to być np. „(iy) żywność składająca się, wyekstrahowana lub produkowana z roślin lub ich części, z wyjątkiem żywności posiadającej historię bezpiecznego stosowania żywności w Unii i składającej się, wyekstrahowanej lub produkowanej z rośliny lub odmiany tego samego gatunku uzyskanych”. Tym samym, to co należy traktować jako nową żywność wynika z rozporządzenia Parlamentu Europejskiego i Rady (UE) nr 2015/2283 z dnia 25 listopada 2015 r. w sprawie nowej żywności, którego przepisy są stosowane od 1 stycznia 2018 r. oraz rozporządzenia wykonawczego Komisji (UE) 2017/2470 z dnia 20 grudnia 2017 r. ustanawiające unijny wykaz nowej żywności zgodnie z rozporządzeniem Parlamentu Europejskiego i Rady (UE) 2015/2283 w sprawie nowej żywności (Dz. Urz. UE L 351 z 30.12.2017, str. 72). Poza tym źródłem informacji na temat statusu określonych składników, jest Katalog Nowej Żywności prowadzony przez Komisję Europejską. Katalog ten to zbiór nazw składników żywności wraz z dostępną w danym momencie informacją o statusie danego składnika, który nie jest zbiorem zamkniętym. Katalog Nowej Żywności (z uwagi na jego charakter) podaje orientacyjne informacje, czy określony składnik pochodzenia zwierzęcego lub roślinnego oraz inne substancje wymagają, czy też nie wymagają, przeprowadzenia postępowania określonego przepisami rozporządzenia nr 2015/2283.
Sąd podkreślił, że analiza strony internetowej https://ec.europa.eu/food/safety/novelfood wskazuje, że w Katalogu Nowej Żywności w odniesieniu do konopi siewnych (Cannabis sativa L.) zamieszczono znak ”V” w kolorze zielonym i następujący opis – w Unii Europejskiej uprawa odmian Cannabis sativa L. jest dozwolona pod warunkiem, że są one zarejestrowane we “Wspólnym katalogu odmian gatunków roślin rolniczych”, a zawartość tetrahydrokanabinolu (THC) nie przekracza 0,2%. Niektóre produkty pochodzące z rośliny Cannabis sativa lub ich części, takie jak nasiona, olej z nasion, mąka z nasion konopi, odtłuszczone nasiona konopi, są powszechnie używane w UE i dlatego nie są nowością. Inne szczegółowe przepisy krajowe mogą ograniczać wprowadzanie do obrotu tego produktu jako żywności lub składnika żywności w niektórych państwach członkowskich. Dlatego zaleca się skonsultowanie się z właściwymi organami krajowymi. Natomiast w odniesieniu do Cannabinoids (Kannabinoidy) zamieszczono znak “X” w kolorze czerwonym i opis – bez uszczerbku dla informacji zawartych w katalogu nowej żywności dla pozycji dotyczącej Cannabis sativa L., ekstrakty Cannabis sativa L. i produkty pochodne zawierające kannabinoidy są uważane za nową żywność, ponieważ nie wykazano historii ich spożycia. Dotyczy to zarówno samych ekstraktów, jak i wszelkich produktów, do których są dodawane jako składnik (np. Olej z nasion konopi). Dotyczy to również ekstraktów z innych roślin zawierających kannabinoidy. Kannabinoidy otrzymywane syntetycznie są uważane za nowe. Z uwagi na powyższe Sąd I instancji podzielił ocenę organu, że w Katalogu Nowej Żywności KE wskazano, że historia spożycia Cannabis sativa L, jako żywności przed dniem 15 maja 1997 r. znana jest tylko w odniesieniu do nasion z konopi, oleju z nasion z konopi, mąki z nasion konopi, odtłuszczonych nasion konopi. Tym samym, zdaniem Sądu I instancji, przed wprowadzeniem do obrotu na terytorium Unii Europejskiej, w odniesieniu do produktu zawierającego w swoim składzie ziele konopi włóknistej konieczne było przeprowadzenie postępowania w sprawie wydania zezwolenia na wprowadzenie nowej żywności na rynek Unii Europejskiej, określonego przepisami rozporządzenia Parlamentu Europejskiego i Rady (UE) Nr 2015/2283 z dnia 25 listopada 2015 r. w sprawie nowej żywności.
Sąd I instancji zwrócił uwagę na fakt różnego statusu prawnego konopi siewnych w poszczególnych państwach członkowskich, co potwierdza interpretację organu zapisów w Katalogu Nowej Żywności prowadzonym przez Komisję Europejską. Organ wykazał bowiem, że w niektórych państwach członkowskich stosowanie konopi siewnych w żywności jest zabronione. Jednocześnie dowody i argumenty Strony mające potwierdzić historię znaczącego spożycia ziela konopi włóknistych w żywności w państwach członkowskich Unii Europejskiej, zdaniem Sądu, nie są wystarczające. Wskazują bowiem na stosowanie w celach leczniczych, a nie jako żywność. Zgodnie zaś z art. 2 rozporządzenia (WE) Nr 178/2002 Parlamentu Europejskiego i Rady z dnia 28 stycznia 2002 r. ustanawiającego ogólne zasady i wymagania prawa żywnościowego środek spożywczy nie obejmuje m.in. produktów leczniczych w rozumieniu dyrektyw Rady 65/65/EWG (1) i 92/73/EWG; narkotyków lub substancji psychotropowych w rozumieniu konwencji o środkach odurzających z 1961 r. oraz Konwencji o substancjach psychotropowych z 1971 r.
Zdaniem Sądu I instancji z opinii Komisji ds. Bezpieczeństwa Żywności i Żywienia Rady Sanitarno – Epidemiologicznej przy GIS z 27 maja 2019 r. wynika m.in., że w przypadku stwierdzenia w produktach z konopi siewnych THC, konieczne jest każdorazowe dokonanie oceny ryzyka, na podstawie przyjętej przez EFSA ostrej dawki referencyjnej. Obowiązek ten nałożony został na przedsiębiorcę. W rozpoznawanej sprawie Skarżąca nie przedstawiła jednak wyników analizy przedmiotowego produktu na obecność i zawartość A9-THC. Rolą organu nie jest zaś prowadzanie dowodów na bezpieczeństwo czy na niebezpieczeństwo środków spożywczych. Unijnym urzędem powołanym do oceny ryzyka w zakresie bezpieczeństwa żywności jest Europejski Urząd ds. Bezpieczeństwa Żywności (EFSA).
Po rozpoznaniu skargi kasacyjnej wniesionej przez Skarżącą Naczelny Sądu Administracyjny wyrokiem z 19 listopada 2021 r, sygn. akt II GSK 1192/21 uchylił wyrok Sądu I instancji i przekazał sprawę do ponownego rozpoznania.
Za zasadny NSA uznał zarzut naruszenia art. 141 § 4 p.p.s.a. bowiem Sąd I instancji nie wyjaśnił z jakich powodów należało uznać, że kontrolowany akt nie jest niezgodny z prawem, a w tym kontekście jakie argumenty miałyby przemawiać za wnioskiem o zaktualizowaniu się w rozpatrywanej sprawie przesłanek wszczęcia postępowania wyjaśniającego, o którym mowa w art. 30 ust. 1 u.b.ż.ż. oraz za przyjęciem, że stanowiący przedmiot powiadomienia produkt jest nową żywnością w rozumieniu rozporządzenia Parlamentu Europejskiego i Rady (UE) nr 2015/2283 w sprawie nowej żywności.
NSA stwierdził, że uzasadnienie zaskarżonego wyroku jest lakoniczne w stopniu uniemożliwiającym poznanie racji i argumentów, którymi kierował się Sąd I instancji stwierdzając, że kontrolowane działanie organu administracji nie jest niezgodne z prawem, co oznacza, że nie realizuje ono nie dość, że funkcji kontroli trafności wydanego w sprawie orzeczenia to również i funkcji perswazyjnej, co w sytuacji, gdyby została ona zrealizowana, a tak jednak nie jest, umożliwiałoby poznanie motywów działania Sądu I instancji mających przekonywać do trafności wydanego w sprawie orzeczenia.
NSA zwrócił uwagę, że jeżeli w rozpatrywanej sprawie kluczowe znaczenie miała odpowiedź na pytanie odnośnie zaktualizowania się przesłanek wszczęcia postępowania wyjaśniającego, o którym mowa w art. 30 ust. 1 u.b.i.ż. oraz odnośnie do tego, czy stanowiący przedmiot powiadomienia Skarżącej produkt jest nową żywnością w rozumieniu rozporządzenia (UE) nr 2015/2283 w sprawie nowej żywności, to za uzasadnione należało uznać oczekiwanie, że Sąd I instancji podda kontroli stanowisko organu administracji we wskazanych kwestiach, w tym w relacji do podważających prawidłowość tego stanowiska argumentów strony skarżącej. Za dowolne zdaniem NSA należało uznać podejście przez Sąd I instancji i przyjęcie w ślad za organem, że tylko i wyłącznie pochodzące z rośliny Cannabis sativa L. lub ich części nasiona, olej z nasion, mąka z nasion konopi, odtłuszczone nasiona konopi — a nie również ziele są powszechnie używane w UE i dlatego nie są nowością.
Zdaniem NSA Sąd I instancji ograniczając się do przywołania treści art. 3 ust. 2 lit. a) rozporządzenia nr 2015/2283 i nie wyjaśniając przy tym w ogóle znaczenia argumentu z przywoływanego li tylko rozporządzenia wykonawczego Komisji (UE) nr 2017/2470 ustanawiającego wykaz nowej żywności, z którego nota bene nie wynika, a Sąd I instancji nie wykazał, że jest inaczej, aby w wykazie tym były produkty zawierające ziele konopi — w odniesieniu do kluczowej argumentacji organu administracji osadzonej na gruncie konsekwencji mających wynikać z treści Katalogu Nowej Żywności prowadzonego przez Komisję Europejską odnośnie do ziela konopi Cannabis sativa L., Sąd i instancji argumentację tę powielił nie odnosząc się przy tym w ogóle do podważających jej prawidłowość argumentów Spółki, które konsekwentnie prezentowane były zarówno w wyjaśnieniach z 26 lutego 2020 r. stanowiących odpowiedź na wezwanie organu, jak i w skardze oraz w piśmie procesowym z 15 września 2020 r., a w konsekwencji — wobec braku ich rozpatrzenia i oceny — w skardze kasacyjnej. W konsekwencji, przyjęcie w ślad za organem administracji, że tylko i wyłącznie pochodzące z rośliny Cannbis sativa L. lub ich części nasiona, olej z nasion, mąka z nasion konopi, odtłuszczone nasiona konopi — a nie również ziele, jak z kolei podnosi to Spółka — są powszechnie używane w UE i dlatego nie są nowością, nie może być ocenione według NSA inaczej, jak tylko, jako arbitralne, a przez to i dowolne. Zwłaszcza, gdy to w relacji do prawnie niewiążącego charakteru Katalogu Nowej żywności, który zawiera niewyczerpującą — a więc otwartą — listę dozwolonych składników (produktów) żywnościowych, która jako pomocnicze źródło służy ich stosownej kwalifikacji, a w konsekwencji poddaniu ich lub nie procedurze zezwolenia zgodnie z rozporządzeniem w sprawie nowej żywności, a także w relacji do celów i zasad tworzenia i uzupełniania wymienionego Katalogu motywowanych potrzebą wyjaśnienia statusu składników (produktów), w odniesieniu do których pojawiają się wątpliwości czy stanowią one nową żywność w rozumieniu przywołanego rozporządzenia, czy też nie, powinna następować rekonstrukcja zawartego w Katalogu Nowej Żywności opisu odnoszącego się do rośliny Cannabis sativa L. oznaczonego ponadto znakiem “V” w kolorze zielonym (zastrzeżonym dla produktów znajdujących się w obrocie jako żywność lub składnik żywności i spożywanych w znacznym stopniu przed 15 maja 1997 r.) oraz znaczenia tego opisu dla odpowiedzi na kluczowe w rozpatrywanej sprawie pytanie.
Rozpoznając sprawę ponownie Wojewódzki Sąd Administracyjny w Warszawie zważył, co następuje:
Skarga zasługuje na uwzględnienie.
Sąd w składzie rozpoznającym niniejszą sprawę miał na uwadze, że Naczelny Sąd Administracyjny wyrokiem z 19 listopada 2021 r. sygn. akt II GSK 1192/21 uchylił wyrok Wojewódzkiego Sądu Administracyjnego w Warszawie z 29 stycznia 2020 r. sygn. akt VII SANVa 1493/20 i przekazał sprawę do ponownego rozpoznania.
Na podstawie art. 190 ustawy z dnia 30 sierpnia 2002 r. Prawo o postępowaniu przed sądami administracyjnymi (Dz. U. z 2019 r., poz. 2325 ze zm.; dalej: “p.p.s.a.”) rozpoznając ponownie sprawę Sąd pozostawał związany oceną prawną oraz wskazaniami co do dalszego postępowania, wyrażonymi w powyżej opisanym wyroku NSA. Podkreślić należy, że wykładnia prawa i wskazania co do dalszego postępowania wyrażone w orzeczeniu sądu wiążą w sprawie nie tylko sąd, lecz także organ, którego działanie, bezczynność lub przewlekłe prowadzenie postępowania było przedmiotem zaskarżenia, a także strony postępowania. Przepis art. 190 p.p.s.a. ma charakter bezwzględnie obowiązujący, co oznacza, że ani organ administracji publicznej, ani sąd, orzekając ponownie w tej samej sprawie, nie mogą nie uwzględnić wykładni prawa dokonanej przez NSA w jego wcześniejszym orzeczeniu, gdyż są nimi związane.
Oceniając postępowanie przeprowadzone przez Głównego Inspektora Sanitarnego podkreślić należy, że w sprawie mamy do czynienia ze szczególną postacią postępowania administracyjnego. Z punktu widzenia zasadniczych funkcji postępowania, tzn. skutków jakie miało wywołać było to postępowanie wyjaśniające, a ze względu na charakter procedury i role stron — postępowanie zbliżone do modelu notyfikacyjnego. Nie są to bezpośrednio pojęcia ustawowe, lecz raczej zaczerpnięte z języka prawniczego — języka czynności i aktów organów sanitarnych i stron dokonujących czynności wobec ww. organów administracji.
Zasadą określoną w art. 29 u.b.ż.ż. jest bowiem to, że podmiot działający na rynku spożywczym, który wprowadza lub ma zamiar wprowadzić po raz pierwszy do obrotu m.in. suplementy diety jest obowiązany powiadomić o tym Głównego Inspektora Sanitarnego. Inicjatywa procesowa należy zatem do wnioskodawcy, który powinien przedstawić kompletne powiadomienie zgodnie z art. 29 ust. 2 u.b.ż.ż, a jednocześnie w ramach tzw. postępowania wyjaśniającego dostarczyć organowi wymaganych informacji. Z kolei, GIS jako organ właściwy ma ocenić kompletność powiadomienia oraz jego zgodność z mającymi zastosowania przepisami prawa obowiązującego: krajowego i unijnego.
Reguły postępowania prowadzonego przez GIS określają tylko art. 30 i 31 u.b.ż.ż. Pierwszy z nich (art. 30 ust. 1 pkt 1 lit. a u.b.ż.ż.) wskazuje, że po otrzymaniu powiadomienia, o którym mowa w art. 29 ust. 1 u.b.ż.ż., Główny Inspektor Sanitarny może przeprowadzić postępowanie mające na celu wyjaśnienie, czy produkt objęty powiadomieniem, ze względu na jego skład, właściwości poszczególnych składników oraz przeznaczenie: jest środkiem spożywczym zgodnie z zaproponowaną przez podmiot działający na rynku spożywczym kwalifikacją oraz czy spełnia wymagania dla danego rodzaju środka spożywczego.
Po tak przeprowadzonym postępowaniu wyjaśniającym, zgodnie z art. 30 ust, 4 u.b.ż.ż., GIS ma obowiązek powiadomić pisemnie podmiot, który dokonał powiadomienia o wynikach przeprowadzonego postępowania, z zastrzeżeniem art. 31 u.b.ż.ż.
Analiza przepisów ww. ustawy wskazuje przy tym, że w ustawie nie zawarto wyraźnego odesłania do przepisów Kodeksu postępowania administracyjnego, stąd ogólne zasady postępowania administracyjnego stosuje się jedynie w takim zakresie, w jakim jest to konieczne dla doprowadzenia do skuteczności powiadomienia o zamiarze wprowadzenia produktu do obrotu, ale nie w szerszym zakresie. W przedmiotowym postępowaniu nie wydaje się decyzji ani postanowień, nie stosuje się przepisów o dwuinstancyjności postępowania, o środkach zaskarżenia decyzji, o udziale stron w postępowania itp. Wskazane art. 29 — 31 u.b.ż.ż. należy zatem uznać za normy szczególne (leges speciales), których zastosowanie powoduje uchylenie norm wynikających z Kodeksu postępowania administracyjnego jako norm ogólnych (leges generali). Nie oznacza to jednak, że skarżąca w ramach przedmiotowego postępowania pozbawiona jest gwarancji procesowych. Należy bowiem mieć na względzie, że także postępowanie wyjaśniające, o którym mowa w art. 30 ust. 1 u.b.ż.ż. powinno spełniać pewne warunki brzegowe, w szczególności czynić zadość podstawowym zasadom zapewniającym zaufanie do władzy publicznej, przy zachowaniu bezstronności, proporcjonalności i równego traktowania.
Jak zaznaczył NSA w ww. wyroku z 19 listopada 2021 r. kluczowe znaczenie w rozpoznawanej sprawie miała odpowiedź na pytanie, czy zaktualizowały się przesłanki wszczęcia postępowania wyjaśniającego, o którym mowa w art. 30 ust. 1 u.b.ż.ż. oraz, czy stanowiący przedmiot powiadomienia skarżącej produkt „Zioła na dobry nastrój” jest nową żywnością w rozumieniu rozporządzenia Parlamentu Europejskiego i Rady (UE) nr 2015/2283 w sprawie nowej żywności. Przedmiotem sporu pozostaje zatem wyłącznie kwestia „nowości” lub nie ziela Cannabis sativa L., jako żywności.
Zgodnie z art. 3 ust. 2 lit. a ww. rozporządzenia nr 2015/2283 „nowa żywność” oznacza żywność, której nie stosowano w znacznym stopniu w Unii do spożycia przez ludzi przed dniem 15 maja 1997 r., która zalicza się do co najmniej jednej ze wskazanych kategorii. Może to być np. “(iv) żywność składająca się, wyekstrahowana lub produkowana z roślin lub ich części, z wyjątkiem żywności posiadającej historię bezpiecznego stosowania żywności w Unii i składającej się, wyekstrahowanej lub produkowanej z rośliny lub odmiany tego samego gatunku uzyskanych”.
Z rozporządzenia Parlamentu Europejskiego i Rady (UE) nr 2015/2283 z dnia 25 listopada 2015 r. w sprawie nowej żywności, którego przepisy są stosowane od 1 stycznia 2018 r. oraz rozporządzenia wykonawczego Komisji (UE) 2017/2470 z dnia 20 grudnia 2017 r. ustanawiającego unijny wykaz nowej żywności zgodnie z rozporządzeniem Parlamentu Europejskiego i Rady (UE) 2015/2283 w sprawie nowej żywności (Dz. Urz. UE L 351 z 30.12.2017, str. 72) wynika zatem, co należy traktować jako nową żywność wynika.
Poza tym źródłem informacji na temat statusu określonych składników, jest Katalog Nowej Żywności, mający prawnie niewiążący charakter, prowadzony przez Komisję Europejską. We wstępie do Katalogu wskazuje się, że zwiera listę niewyczerpująca i służy jako wskazówka, czy dany produkt będzie wymagał zezwolenia zgodnie z rozporządzeniem w sprawie nowej żywności.
Zatem Katalog ten to zbiór nazw składników żywności wraz z dostępną w danym momencie informacją o statusie danego składnika, który nie jest zbiorem zamkniętym. Katalog Nowej Żywności (z uwagi na jego charakter) podaje orientacyjne informacje, czy określony składnik pochodzenia zwierzęcego lub roślinnego oraz inne substancje wymagają, czy też nie wymagają, przeprowadzenia postępowania określonego przepisami rozporządzenia nr 2015/2283.
W zaskarżonym akcie, GIS odwołując się do ww. Katalogu uznał, że w przypadku rośliny Cannabis sativa L. znana jest historia spożycia przed dniem 15 maja 1997 r., jako żywności tylko następujących produktów: nasion, oleju z nasion konopi, mąki z nasion konopi, odtłuszczonych nasion konopi. Zdaniem organu produkty pochodzące z konopi siewnych innych niż ww. uważane są za nową żywność, co oznacza, że przed wprowadzeniem do obrotu na terytorium UE w tym Polski, jako żywność produktu zawierającego w swoim składzie ziele konopi włóknistej, konieczne jest przeprowadzenie postępowania w sprawie wydania zezwolenia na wprowadzenie nowej żywności na rynek Unii Europejskiej określonymi przepisami rozporządzenia nr 2015/2283.
Formułując taki wniosek organ nie uwzględnił jednak, że w na stronie internetowej Komisji Europejskiej pod adresem https://ec.europa.eufroodisafetyinovel_food w udostępnionym Katalogu Nowej Żywności, można sprawdzić nazwę składnika żywności wraz z informacją o statusie danego składnika. Status składnika jest określony za pomocą symboli. Symbol V oznacza, że produkt znajdował się w obrocie jako żywność lub składnik żywności oraz był spożywany w znacznym stopniu przed 15 maja 1997 r., a więc jego wprowadzanie do obrotu nie jest przedmiotem Rozporządzenia (EC) nr 258/97 (a obecnie 2015/2283). Dla składnika, którym jest roślina z gatunku Cannabis sativa L., czyli konopie siewne Komisja Europejska zamieściła symbol V w kolorze zielonym i następujący opis – w Unii Europejskiej uprawa odmian Cannabis sativa L. jest dozwolona pod warunkiem, że są one zarejestrowane we “Wspólnym katalogu odmian gatunków roślin rolniczych”, a zawartość tetrahydrokanabinolu (THC) nie przekracza 0,2%. Niektóre produkty pochodzące z rośliny Cannabis sativa lub ich części, takie jak nasiona, olej z nasion, mąka z nasion konopi, odtłuszczone nasiona konopi, są powszechnie używane w UE i dlatego nie są nowością.
Zgodnie zatem z powyższym roślina ta (bez wskazania na określone części i bez wyłączenia jakiejkolwiek części, o czym świadczy sformułowanie „roślina lub jej części”) ma historię stosowania i nie stanowi nowej żywności. Poza tym, pod składnikiem zostały wymienione przykładowe produkty (na co jednoznacznie wskazuje sformułowanie z ang. „such as” — „takie jak”), które można otrzymać z tej rośliny. Jest to zatem niewyczerpująca, a więc otwarta lista dozwolonych składników (produktów) żywnościowych i służy jako wskazówka, czy dany produkt będzie wymagał zezwolenia zgodnie z rozporządzeniem w sprawie nowej żywności
Twierdzenie w tej sytuacji przez GIS, ze w ww. Katalogu wyraźnie wskazano, że w przypadku rośliny Cannabis sativa L. znana jest historia spożycia przed dniem 15 maja 1997 r. jako żywności tylko następujących produktów: nasion z konopi, oleju z nasion konopi, mąki z nasion konopi, odtłuszczonych nasion konopi, stanowiło nieuprawnioną nadinterpretację stanowiska Komisji Europejskiej. Wskazać w tym miejscu wypada, że w Katalogu Nowej żywności są wprost wymienione produkty z konopi, które dnia 15 stycznia 2019 r. Komisja Europejska uznała za nową żywność i opatrzyła symbolem „X” w kolorze czerwonym, który zgodnie z legendą oznacza, że odnośnie do danego produktu zostało skierowane zapytanie, czy wymaga on autoryzacji zgodnie z rozporządzeniem nr 2015/2238 w sprawie nowej żywności i że zgodnie z informacjami dostępnymi właściwym organom państw członkowskich, ten produkt nie był stosowany jako żywność lub składnik żywności przed dniem 15 maja 1997 r. Nową zatem żywnością, jak wynika z Katalogu są, bez uszczerbku dla wpisu dotyczącego Cannabis sativa L., wyłącznie: 1. ekstrakty z rośliny Cannabis sativa L. zawierające kannabinoidy; 2. produkty pochodzące z tych ekstraktów, a więc wszelkie produkty do których te ekstrakty zostały dodane (takie jak np. olej z nasion), 3. ekstrakty z innych roślin niż Cannabis sativa L. zawierające kannabinoidy, 4. syntetycznie otrzymane kannabinoidy.
Zatem ziele Cannabis sativa L. na tej liście nie zostało wymienione. Za nieuprawnione należało więc uznać twierdzenie GIS, że stanowisko Komisji Europejskiej zamieszczone w Katalogu Nowej Żywności w odniesieniu do innych części konopi siewnych niż nasiona jest w tej kwestii jednoznaczne. Oznacza to, że dokonana przez GIS interpretacja zapisów Katalogu Nowej Żywności w kontekście „nowości” ziela Cannabis sativa L., jako żywności była wadliwa. Rację ma więc skarżąca, że stanowisko GIS jest błędne. Katalog z założenia nie wymienia wszystkich produktów żywnościowych oraz ich składników, jakie mogą być wykorzystywane do produkcji żywności. To, że dany produkt spożywczy lub składnik nie jest w nim wprost wymieniony, nie świadczy o tym, że automatycznie jest on nową żywnością. W Katalogu Nowej Żywności są wymienione wyłącznie te produkty i składniki, co do których Komisja Europejska dostała zapytanie o opinię czy dany produkt lub składnik powinien przejść procedurę autoryzacji. O tym stanowi wprost legenda objaśniająca status poszczególnych składników.
Definitywne stwierdzenie „nowości” ziela Cannabis sativa L., jako żywności przez organ było niemożliwe także z tego powodu, że z przedłożonej przez skarżącą opinii Komisji Europejskiej z dnia 18 grudnia 1997 r., znanej także organowi z urzędu, wprost wynikało wyłączenie ziela Cannabis sativa L. spod obowiązywania rozporządzenia w sprawie nowej żywności. Wskazano w niej bowiem, że „zdecydowano, iż żywność zawierająca części ziela konopi siewnej nie podlega pod regulację Rozporządzenia (WE) nr 258/97 Parlamentu Europejskiego i Rady ws. Nowej żywności” (tj. rozporządzenia zastąpionego w 2015 r. nowym rozporządzeniem Parlamentu Europejskiego i Rady (UE) nr 2015/2283).
Z zaskarżonego pisma GIS nie wynika, by organ w jakikolwiek sposób analizował i odniósł się do ww. opinii, stwierdzając jedynie, że wobec wielokrotnej weryfikacji statusu prawnego Cannabis sativa L. na posiedzeniach Komisji Europejskiej w ramach grupy roboczej ds. nowej żywności, jest ona nieaktualna. Tymczasem załączone przez skarżącą do skargi kasacyjnej od wyroku tut. Sądu z 29 stycznia 2021 r. dokumenty wskazują, że odpowiadając na pismo GIS z 14 kwietnia 2017 r. Komisja Europejska stwierdziła, że stanowisko uzgodnione w grudniu 1997 r., zawarte w opinii pozostaje aktualne i nie zostało odwołane oraz, że zgodnie z Katalogiem Nowej Żywności, rozporządzenie (WE) nr 258/97 nie ma zastosowania do większości żywności i składników żywności pochodzących z Cannabis sativa L., a za nową żywność uznaje się ekstrakty z Cannabis sativa wzbogacone kannabidiolem (CBD). Zarówno pismo GIS z 14 kwietnia 2017 r. skierowane do Komisji, w którym organ podnosił w istocie te same wątpliwości i argumenty, jak w zaskarżonym akcie z 15 maja 2020 r., jak i odpowiedź Komisji Europejskiej były organowi znane w dacie złożenia przez skarżącą zawiadomienia o zamiarze wprowadzenia po raz pierwszy na terytorium PR jako suplementu diety produktu pn. Zioła na dobry nastrój, niemniej jednak nie zostały przez organ ujawnione, a tym samym poddane jakiejkolwiek analizie, w kontekście ustalenia, czy wobec aktualności opinii Komisji z 1997 r. zachodziły przesłanki do wszczęcia postępowania wyjaśniającego. Tymczasem skarżąca w toku postępowania w piśmie z 26 lutego 2020 r. dla wykazania, że żywność zawierająca składniki roślinne konopi włóknistych nie jest objęta rozporządzeniem w sprawie nowej żywności załączyła trzy dokumenty z dnia 3 lutego 1998 r., 3 marca 1998 r. oraz 15 maja 2017 r. w których Komisja Europejska powoływała się na tę opinię.
Zgodnie z punktem 17 preambuły rozporządzenia nr 2015/2283 w sprawie nowej żywności: „żywność wyprodukowana wyłącznie ze składników żywności, które nie są objęte zakresem stosowania niniejszego rozporządzenia […] nie powinna być uważana za nową żywność”.
Jeśli zatem produkty spożywcze zawierające lub składające się z ziela Cannabis sativa L., w tym przypadku produkt, którego dotyczyło powiadomienie skarżącej nie jest objęty zakresem rozporządzenia nr 2015/2283 w sprawie nowej żywności, to nie było konieczne przeprowadzenie postępowania w sprawie wydania zezwolenia na wprowadzenie nowej żywności na rynek w Unii Europejskiej.
Za wątpliwe należy uznać zadaniem Sądu, również stanowisko GIS jakoby na przestrzeni ostatnich lat status Cannabis sativa L. oraz kannabinoidów był dyskutowany na posiedzeniach na poziomie Komisji Europejskiej w ramach grupy roboczej, a także grupy roboczej ds. aromatów, co miałoby świadczyć o nieaktualności powoływanej opinii Komisji Europejskiej z 18 grudnia 1997 r. Organ w tych twierdzeniach pozostaje zupełnie gołosłowny, bowiem nie załączył do akt żadnych dokumentów, w tym tych z posiedzeń grupy roboczej, na które się powoływał i wywodził argumenty o konieczności decydowania o statusie ziela konopi siewnych jako nowej żywności wymagającej procedury rejestracyjnej określonej rozporządzeniem w sprawie nowej żywności. Tymczasem skarżąca wskazywała, że z raportów z posiedzeń Komisji Europejskiej wynikało jednoznacznie, że dyskusje grup roboczych nie dotyczyły ziela konopi, a jedynie ekstraktów z konopi wzbogaconych CBD.
Niezależnie jednak od tego, co było przedmiotem prac grup roboczych, to nie można byłoby i tak orzekać o nieaktualności opinii Komisji Europejskiej z 1997 r. na podstawie samego tylko faktu, że miały na nich miejsce dyskusje przedstawicieli państw członkowskich, bowiem ich przedmiotem były jedynie opinie przedstawicieli państw członkowskich, a nie stanowisko Komisji. Rację ma również skarżąca, że nie ma formalnie znaczenia dla aktualności opinii z 1997 r., jakie wpisy zostały zamieszczone w Katalogu Nowej żywności, ponieważ Katalog ten nie zawiera opinii Komisji Europejskiej. W opisie Katalogu Nowej żywności dostępnym na stronie internetowej wskazano bowiem, że „informacje publikowane w Katalogu Nowej żywności pochodzą z przekazów poszczególnych państw członkowskich”. Zmiany wprowadzane w Katalogu nie są więc w żadnej mierze opinią Komisji, a jedynie zbiorem doniesień od poszczególnych państw członkowskich.
Przypomnieć należy, że zgodnie z art. 2 ust. 1 rozporządzenia nr 2015/2283, dotyczy ono wprowadzania do obrotu we Wspólnocie wyłącznie takiej żywności i składników żywności, które dotychczas nie były w znacznym stopniu wykorzystywane do spożycia przez ludzi, a które dodatkowo zaliczają się do dziesięciu wymienionych w rozporządzeniu kategorii. W przypadku żywności i składników żywności, które nie należą do jednej z kategorii wymienionych w art. 3 ust. 2 a) rozporządzenia nr 2015/2283, nie może aktualizować się obowiązek przedstawienia jakichkolwiek dokumentów, w tym dowodów historii spożycia tej żywności lub składnika żywności, o których mowa w art. 4 ust. 2 rozporządzenia oraz art. 121 ust. 1 u.b.ż.ż., gdyż tego rodzaju produkty nie są objęte przepisami rozporządzenia nr 2015/2283.
Zatem konieczność przeprowadzenia dowodów na okoliczność znacznego spożycia ziela konopi siewnych przed 1997 r. powinna pojawić się dopiero w sytuacji, gdyby z opinii Komisji Europejskiej, wypracowanych stanowisk państw członkowskich w ramach grupy roboczej oraz mającego charakter pomocniczy Katalogu Nowej żywności rzeczywiście wynikało, że produkty na bazie Cannabis sativa L. podpadają pod regulację rozporządzenia w sprawie nowej żywności.
W tym zakresie jak wspomniano organ pominął opinię Komisji Europejskiej, dokonując jednocześnie wadliwej interpretacji zapisów Katalogu Nowej żywności dotyczących konopi siewnych, a w konsekwencji błędnie zdaniem Sądu za niewystarczające uznał dowody i argumenty skarżącej, zawarte w piśmie z 26 lutego 2020 r, wskazujące na historię znaczącego spożycia ziela konopi włóknistych w żywności w celu żywienia ludzi w państwach członkowskich Unii Europejskiej. Skarżąca w piśmie tym omówiła i przedstawiła bogaty biblioteczny spis źródeł, w których wskazuje się na spożycie ziela konopi włóknistych od setek tysięcy lat. Wskazała przykłady spożywania ziela konopi w normalnej diecie we Włoszech, Niemczech, Szwajcarii, jak i w Polsce.
O ile zgodzić się należy z organem, że w świetle prawa żywnościowego środki spożywcze, w tym suplementy diety nie mogą posiadać właściwości charakterystycznych dla produktów leczniczych w rozumieniu przepisów prawa farmaceutycznego, to niewątpliwie dowody przedstawione przez stronę w ramach przedmiotowego postępowania wskazywały historię spożycia ziela konopi włóknistych zarówno jako żywności, jak i celem suplementacji normalnej diety zgodnie z definicją żywności zawartą w rozporządzeniu (WE) nr 178/2002 Parlamentu Europejskiego i Rady z dnia 28 stycznia 2002 r. ustanawiającego ogólne zasady i wymagania prawa żywnościowego (…) (Dz. U.L31 z 1.2.2002, s1, ze zm. oraz definicją suplementów diety zawartą w Dyrektywie 2002/46/WE Parlamentu Europejskiego i Rady z dnia 10 czerwca 2002 r. w sprawie zbliżenia ustawodawstw Państw Członkowskich odnoszących się do suplementów żywnościowych (Dz. U. 2006 Nr 171 poz, 1225, ze zm.) oraz u.b.ż.t. Nie jest zatem tak jak wskazuje GIS, że w większości przypadków przedstawione przez skarżącą dowody wskazywały, że ziele konopi było stosowane w celach leczniczych, a nie jako żywność. Przy czym rację ma skarżąca, że zgodnie ze stanowiskiem Rady Europy wszystkie zioła mają dwojakie zastosowanie: lecznicze i spożywcze (w tym jako suplement diety), a rozróżnienie obu kategorii w tej mierze polega jedynie na ilości oraz celu spożycia (por. stanowisko Rady Europy wyrażone w artykule zlokalizowanym pod adresem internetowym: http://www. dgv. minagricultura.ptixeov21/attacheflieu.jsp?look_parentBoui=19553032&alt display.n&att_download=y), co niejako przyznaje sam organ stwierdzając na str. 6 zaskarżonego aktu, że także melisa i waleriana mają swoje dawki terapeutyczne i nieterapeutyczne (stosowane w suplementach), wobec czego oba zioła mają zastosowanie żywieniowe i lecznicze – zależnie od ilości i celu spożycia.
W zaskarżonym piśmie organ bez żadnej głębszej analizy, jednym zdaniem stwierdził, że dowody przedstawione przez skarżącą nie są wystarczające, by potwierdzić historię znaczącego spożycia ziela konopi włóknistych w celu żywienia ludzi w państwach członkowskich UE, co powoduje, jak słusznie podnosi skarżąca brak możliwości oceny argumentów organu. Organ nie skomentował również w żaden sposób powoływanej przez skarżąca uchwały nr 171/2017 Rady Ministrów z 26 października 2017 r. w sprawie ustanowienia programu wieloletniego pod nazwą „Odbudowa i zrównoważony rozwój produkcji oraz przetwórstwa naturalnych surowców włóknistych dla potrzeb rolnictwa i gospodarki”. Tymczasem Program ten wykazuje, że „produkty uboczne z przerobu lnu i konopi włóknistych takie jak kwiatostany, nasiona, plewy, paździerze, są wartościowym źródłem bioaktywnych związków i substancji, w tym nienasyconych kwasów tłuszczowych omega-3 i omega-6, aminokwasów, witamin i śluzów roślinnych, suplementów paszowych i surowcem do wytwarzania ekologicznych kompozytów”. Podkreślić przy tym należy, że ww. uchwała została oparta m.in. o ustawę z dnia 25 sierpnia 2006 r. o bezpieczeństwie żywności i żywienia, ustawę z dnia 29 lipca 2005 r. o przeciwdziałaniu narkomanii (Dz. U. z 2017 r. poz. 783, ze zm.) oraz rozporządzenie (WE) nr 178/2002 Parlamentu Europejskiego i Rady z dnia 28 stycznia 2002 r. ustanawiające ogólne zasady i wymagania prawa żywnościowego, powołującego Europejski rząd do Spraw Bezpieczeństwa Żywności oraz ustanawiające procedury w zakresie bezpieczeństwa żywności (Dz. Urz. WE L 31 z 01.02.2002, str. 1, ze zm. – Dz. Urz. UE Polskie wydanie specjalne, rozdz. 15, t. 6, str. 463).
Jednym z celów tego programu jest wzrost areału upraw konopi włóknistych o potencjale medycznym, w powiązaniu z wytworzeniem nowych specjalistycznych produktów farmaceutycznych, suplementów diety i żywności funkcjonalnej na rynku, co przyczyni się do poprawienia zdrowia populacji zagrożonej chorobami cywilizacyjnym.
Zatem GIS w ramach, jak wskazuje w zaskarżonym akcie, podejmowanych działań mających na celu zapewnienie wysokiego poziomu ochrony zdrowia i życia ludzi oraz ochronę konsumentów winien odnieść się do powoływanych przez skarżącą argumentów w zakresie przestrzegania założeń ww. programu, zwłaszcza jeśli skarżąca z powyższego wywodziła korzystne dla siebie skutki prawne.
Tymczasem, jak wynika z zaskarżonego pisma organ zanegował wartość dowodową wyłącznie jednego z powołanych przez skarżąca aktów świadczących o spopularyzowanym w krajach Unii Europejskiej spożyciu konopi włóknistych i tym samym braku przeciwskazań do obrotu produktami spożywczymi na bazie Cannabis sativa L. Chodzi tu o rozporządzenie Ministra Rolnictwa i Rozwoju Wsi Republiki Słowackiej nr 309/2015 z 4 listopada 2015 r., w którym określono listę roślin i jej części, które mogą być składnikami herbat. Organ stanął na stanowisku, że dopuszczenie do spożycia liści i nasion konopi w ramach naparu herbacianego nie stanowi o „znaczącym spożyciu”, a co najwyżej o dopuszczalności specjalnego stosowania spożywczego wyłącznie tylko części konopi (liści i nasion). Nie wyjaśnił przy tym z jakiej przyczyny dopuścił zastosowanie tylko nasion, a zanegował spożycie liści i kwiatów i na jakiej podstawie uznał, że spożycie naparu herbacianego należy dyskwalifikować z przykładu zastosowania spożywczego.
Skarżąca powołując powyższy akt słusznie dowodziła, że interpretacja Katalogu Nowej Żywności powinna uwzględniać to, że w państwach członkowskich nie ograniczono się tylko do zezwolenia na spożycie nasion, które katalog wprost wymienia. Skarżąca próbowała w ten sposób, słusznie zresztą, wykazać otwartość zapisów Katalogu i jego definitywność wyłącznie w zakresie znaczeń wykluczających tj. czerwonych znaków „X”, o czym była mowa wyżej.
Powyższa argumentacja w zakresie oceny treści dowodów przedstawionych przez skarżąca, już po wszczęciu postepowania wyjaśniającego, wskazuje na wadliwość działania organu. Należy bowiem pamiętać, że decydujące znaczenie w tej sprawie miała jedynie kwestia statusu Cannabis sativa L. jako żywności nowej, bądź nie. Z tej też przyczyny bez znaczenia dla oceny tego statusu pozostawały rozważania organu (zawarte w odpowiedzi na skargę), czy w jakimkolwiek innym kraju obowiązuje zakaz stosowania ziela konopi siewnej w żywności, a także argumenty o „niebezpieczności” produktu skarżącej. Organ w tej ostatniej kwestii wskazał na str. 5 zaskarżonego aktu z 15 maja 2020 r., że „wprowadzenie do obrotu jako żywności suszu z konopi siewnych może stanowić potencjalne zagrożenie dla konsumenta ze względu na zawartość THC, ponieważ wszystkie rośliny konopi siewnych mogą zawierać fitokannabinoidy”. Jakkolwiek w odpowiedzi na skargę organ wyjaśnił, że nie stwierdził, by produkt skarżącej był niebezpieczny, to istotnie rodzi się pytanie w jakim celu organ podnosił te argumenty, skoro zawartość THC w suplemencie skarżącej nie stanowiła przedmiotu postępowania toczącego się przez organem.
W świetle powyższego zgodzić się należało ze skarżącą, że organ najpierw wadliwie zinterpretował zapisy Katalogu Nowej żywości prowadzonym przez Komisję Europejską dotyczących konopi siewnych, a następnie przeprowadził niepełne i ograniczone do minimum postępowanie dowodowe, pomijając przy tym dowody z dokumentów złożone przez skarżącą, a także dowody wytworzone przez sam organ i znane mu z urzędu, w tym stanowisko zawarte w opinii Komisji Europejskiej z 18 grudnia 1997 r. oraz dokumentach pochodzących od jej przedstawicieli z 3 lutego 1998 r., 3 marca 1998 r. i 15 maja 2017 r., złożonych przez skarżącą przy piśmie z 26 lutego 2020 r., w których Komisja Europejska powołuje się na ww. opinię. W efekcie takiego działania organ w sposób zupełnie dowolny stwierdził, że ziele Cannabis sativa L. stanowi nową żywność w rozumieniu rozporządzenia nr 2015/2283 w sprawie nowej żywności i wymaga zezwolenia na wprowadzenie na rynek UE, przez co naruszył także art. 6 ust. 2 rozporządzenia w sprawie nowej żywności.
W tym stanie rzeczy Wojewódzki Sąd Administracyjny w Warszawie, na podstawie art. 146 ust. 1 p.p.s.a. uchylił zaskarżony akt, orzekając, jak w punkcie I sentencji wyroku. O kosztach postępowania orzeczono na podstawie art. 200 p.p.s.a. w zw. z art. 205 § 2 p.p.s.a. i § 14 ust. 1 pkt 1 lit. c rozporządzenia Ministra Sprawiedliwości z 22 października 2015 r. (Dz. U. z 2018 r. poz. 265 ze zm.) w sprawie opłat za czynności radców prawnych.
Wskazania co do dalszego postępowania wynikają wprost z przedstawionych rozważań i sprowadzają się do konieczności ponownego, dokładnego rozpoznania sprawy w jej całokształcie, na podstawie prawidłowo i wyczerpująca przeprowadzonej analizy, która powinna być jednoznaczna i spójna oraz przedstawiona w sposób umożliwiający ustalenie toku rozumowania organu. Stwierdzenie braku podstaw do prowadzenia postępowania wyjaśniającego powinno skutkować umorzeniem postępowania w tej materii.
Sprawę rozpoznano i wyrok wydano na posiedzeniu niejawnym, na podstawie art. 15zzs4 ust. 3 ustawy o COVID-19. Zgodnie z tym przepisem przewodniczący może zarządzić przeprowadzenie posiedzenia niejawnego, jeżeli uzna rozpoznanie sprawy za konieczne, a przeprowadzenie wymaganej przez ustawę rozprawy mogłoby wywołać nadmierne zagrożenie dla zdrowia osób w niej uczestniczących i nie można przeprowadzić jej na odległość z jednoczesnym bezpośrednim przekazem obrazu i dźwięku. Na posiedzeniu niejawnym w tych sprawach sąd orzeka w składzie trzech sędziów. W będącej przedmiotem kontroli sądowej sprawie Przewodniczący Wydziału zarządzeniem z 11 lutego 2022 r. skierował sprawę do rozpoznania na posiedzeniu niejawnym.
PSSST – skoro już tu dotarłaś/eś, to może skusisz się na Zioła na Dobry Nastrój, albo jakiś olejek 😉 ?